COPD und Asthma - Definition und Abgrenzung
Asthma und COPD sind zwei völlig verschiedene Erkrankungen. Sie unterscheiden sich in Ursachen, Verlauf und Prognose. Diese obstruktiven Erkrankungen von Lunge und Atemwegen erfordern trotz ähnlicher Symptome (Luftnot!) unterschiedliche Therapien. Die Differenzialdiagnose ist daher außerordentlich wichtig. Da es sich um häufig vorkommende Erkrankungen mit immer größerer sozioökonomischer Bedeutung — also echte Volkskrankheiten — handelt, stehen im Internet nationale Versorgungsleitlinien für Asthma und COPD zur Verfügung.
COPD
Die nationale Versorgungsleitlinie COPD definiert den Begriff COPD (Chronic Obstructive Pulmonary Disease) wie folgt: „Die COPD umfasst eine Symptomatik und funktionelle Beeinträchtigung der Lunge, die charakterisiert ist durch eine Kombination aus chronischem Husten, gesteigerter Sputumproduktion, Atemnot, Atemwegsobstruktion und eingeschränktem Gasaustausch. Die COPD lässt sich als eine Krankheit definieren, die durch eine progrediente, nach Gabe von Bronchodilatatoren und/oder Corticosteroiden nicht vollständig reversible Atemwegsobstruktion auf dem Boden einer chronischen Bronchitis und/oder eines Lungenemphysems gekennzeichnet ist.“
Andere obstruktive Erkrankungen
Nicht eingeschlossen in die Diagnose COPD werden andere Ursachen einer chronischen Atemwegsobstruktion. Dazu zählen Erkrankungen wie Mukoviszidose (Erbkrankheit), Bronchiektasie und Bronchiolitis obliterans.
chronische Bronchitis
Nach WHO-Definition liegt eine chronische Bronchitis dann vor, wenn Husten und Auswurf über wenigstens 3 Monate in mindestens 2 aufeinanderfolgenden Jahren bestehen. Eine chronisch obstruktive Bronchitis ist durch eine im Regelfall permanente Atemwegsobstruktion gekennzeichnet, die keine große Variabilität aufweist.
Lungenemphysem
Das Lungenemphysem wird pathologisch-anatomisch definiert als irreversible Erweiterung und Destruktion der Lufträume distal der terminalen Bronchiolen. Es geht bei den meisten Erkrankten mit einer funktionell relevanten Atemwegsobstruktion einher. Zwischen dem Ausmaß der Destruktion im alveolären Bereich (Lungenbläschen) und der messbaren Atemwegsobstruktion (Lungenfunktion) besteht eine schlechte Korrelation. Mit Hilfe der Computertomographie des Brustkorbs (Thorax-CT) gelingen im Regelfall eine Differenzierung des vorherrschenden Typs und die Charakterisierung des regionalen Destruktionsgrades der Lungenabschnitte infolge des Emphysems.
Pathologisch-anatomisch wird das Lungenemphysem wie folgt eingeteilt:
zentrilobuläre (zentroazinäre) Emphysem
Das zentrilobuläre (zentroazinäre) Emphysem entsteht typischerweise aus einer chronisch obstruktiven Bronchitis. Dieser Typ ist primär in den Oberlappen der Lunge zu finden. Meist handelt es sich um Raucher oder ehemalige Raucher. Bei diesem Emphysem sind zunächst die feinen Verästelungen der Bronchien, die direkt zu den Alveolen führen, betroffen. Die Schädigung der Lungenbläschen (Alveolen) beginnt im Bereich der kleinen Atemwege und breitet sich im weiteren Verlauf innerhalb der kleinsten funktionellen Lungeneinheit — so genannter sekundärer Lobulus - von zentral nach peripher aus.
panlobuläre (panazinäre) Emphysem
Das panlobuläre (panazinäre) Emphysem betrifft typischerweise primär die Lungenbläschen und erst später die kleineren Atemwege. Die Destruktion im sekundären Lobulus schreitet meist von peripher nach zentral fort. Hauptgrund für die Entstehung eines panlobulären Emphysems ist der vererbte Mangel des Enzyms Alpha-1-Antitrypsin. Dieses Enzym schützt die Lunge vor zerstörerisch wirksamen Proteasen, die das Gewebe bei Enzymmangel angreifen können.
paraseptale Emphysem
Das paraseptale Emphysem entsteht in der Peripherie der Lunge und bevorzugt im Bereich der Lungenspitzen.
Wenn die Alveolarsepten einreißen, können die Emphysemblasen zusammenfließen. Es bilden sich bei weiterem Wachstum größere Blasen, so dass ein bullöses Emphysem entsteht.
Die Erkennung von Frühstadien der COPD oder eines Lungenemphysems ist selbst bei Einsatz modernster Lungenfunktionsgeräte sowie der Computertomographie des Brustkorbs schwierig. In fortgeschrittenen Stadien der Erkrankung erscheint die Unterscheidung zwischen dem Schweregrad der chronisch obstruktiven Bronchitis und dem Schweregrad und Verteilungsmuster des Lungenemphysems mittels differenzierter Lungenfunktionsanalyse und bildgebender Diagnostik — hier insbesondere mit Hilfe der hochauflösenden CT-Verfahren - auch im Hinblick auf die optimale Nutzung vorhandener Therapieoptionen sinnvoll.
Ursachen der COPD
COPD wird in erster Linie durch Rauchen verursacht. Doch kommen auch andere Ursachen in Betracht, zum Beispiel Feinstäube wie Ruß, Rauch und diverse Schadstoffe am Arbeitsplatz, z.B. Quarzstaub. Erstes Anzeichen der Erkrankung ist Husten, der mit der Zeit immer hartnäckiger wird und die Betroffenen vor allem morgens quält. Hinzu kommt Auswurf, der langsam zäher wird und immer schwerer abzuhusten ist. Die Patienten leiden unter Atemnot, zunächst nur bei Belastung, später auch in Ruhe. Die Krankheit nimmt im Regelfall einen progredienten Verlauf.
Die Diagnose richtet sich nach den Beschwerden des Patienten, in erster Linie aber nach den Ergebnissen der Lungenfunktionsprüfung. Die Häufigkeit des schubweisen Ausbruchs (auch Exazerbation genannt) ist ein wesentliches Diagnosekriterium. Die folgende Einteilung (Tabelle 1) wurde von der Global Initiative for Chronic Obstructive Lung Disease (GOLD) veröffentlicht.
Schweregrad der COPD anhand der Obstruktion:
Bei Patienten mit einem FEV1/FVC < 0.70:
GOLD 1: Leicht FEV1 > 80% Soll
GOLD 2: Moderat 50% < FEV1 < 80% Soll
GOLD 3: Schwer 30% < FEV1 < 50% Soll
GOLD 4: Sehr schwer FEV1 < 30% Soll
Tabelle 1 aus GOLD 2011
Abkürzungen:
FEV1 = forciertes exspiratorisches Volumen in einer Sekunde „Einsekundenluft“ hier nach Anwendung eines bronchienerweiternden Medikamentes
FVC = forcierte Vitalkapazität
Ende 2011 wurde eine neue Klassifizierung der COPD durch die Global Initiative for Chronic Obstructive Lung Diseases (GOLD-Experten) vorgeschlagen. Sie berücksichtigt neben der spirometrischen Einteilung mit Hilfe des Tiffenau-Wertes — auch FEV1 oder Einsekundenluft genannt - (siehe Tabelle 1) zwei weitere Kriterien: die krankheitsbezogene Lebensqualität anhand des CAT-Scores (COPD Assessment Test) oder den Dyspnoegrad gemäß MRC-Skala einerseits und die Exazerbationsrate im zurückliegenden Jahr andererseits. So entsteht eine Vierfeldertafel (Abbildung 1 und Tabelle 2) mit Einteilung der COPD in die 4 Schweregrade A-D. Diese neue Einteilung wird auf dem Symposium 2013 in Hattingen detaillierte vorgestellt.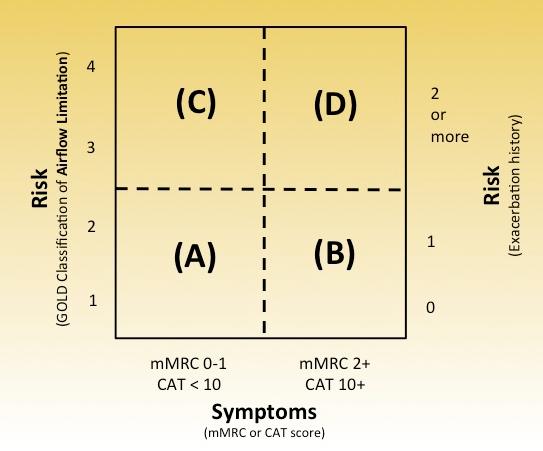
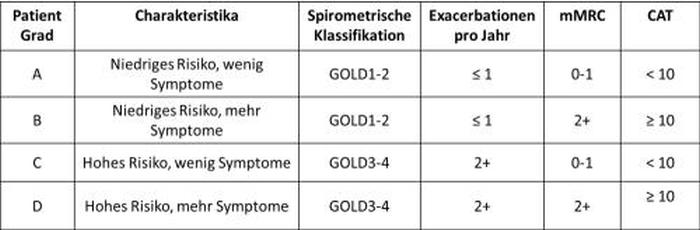
Abbildung 1 und Tabelle 2 nach GOLD 2011 (Einzelheiten siehe Text)
Nach wie vor erfolgt zunächst die Einteilung der COPD in die Stadien I-IV anhand der Lungenfunktion (Tabelle 1). Wichtig ist der Grenzwert der FEV1 von 50%. Beträgt der Wert ≥50%, so wird von einem Schweregrad A oder B gesprochen. Bei einem FEV1-Wert <50%, liegt der Schweregrad C oder D vor (Abbildung 1, Tabelle 2). Für die Zuordnung der Schweregrade kann darüber hinaus die Exazerbationsrate herangezogen werden. Da eine höhere Exazerbationsrate in der Vergangenheit mit einem höheren Risiko in der Zukunft vergesellschaftet ist, werden Patienten mit einer Exazerbationsrate von ≥2 pro Jahr ebenfalls den Gruppen C und D zugeteilt. Dies gilt auch dann, wenn die Lungenfunktion noch relativ gut erhalten ist (FEV1 ≥50%).
Berücksichtigt man alle Kriterien, so kann hierdurch zwischen den Gruppen mit niedrigem Risiko (Gruppen A und B) und den Gruppen mit hohem Risiko (Gruppe C und D) unterschieden werden. Darüber hinaus wird als weitere Dimension die Lebensqualität mit herangezogen, welche durch die mMRC (modified Medical Research Counsil Dyspnea Scale) (Abbildung 2) oder den CAT (COPD Assesment Test) (Abbildung 3) bestimmt werden kann. Die festgesetzte Grenze des CAT liegt bei ≥10, die der mMRC bei ≥2.

Abbildung 2: Atemnotskala nach MRC
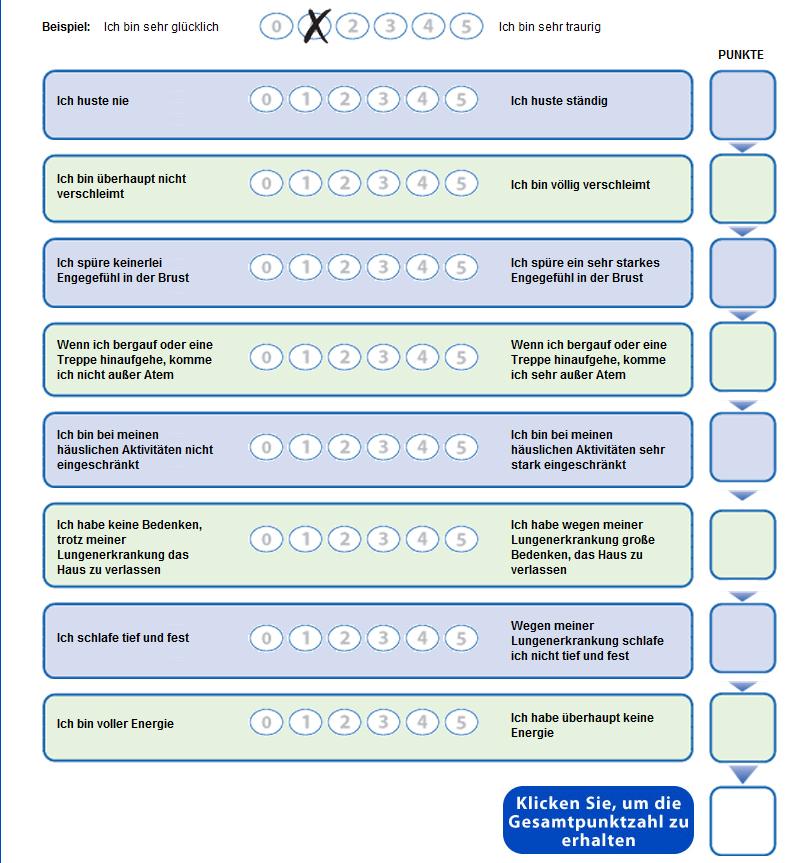
Abbildung 3: Beurteilung der spezifischen Lebensqualität mit Hilfe des CAT
Bei Erreichen dieser Grenzen geht man von einer relevanten Beeinträchtigung der Lebensqualität aus, sodass die Patienten dann den Gruppen B oder D zugeordnet werden und nicht den Gruppen A und C (Abbildung 1). Mit Hilfe der neuen Einteilung wird die Komplexität des Krankheitsbildes COPD besser erfasst. Es ist davon auszugehen, dass das Therapiekonzept bei COPD unter Berücksichtigung der Lebensqualität und der körperlichen Leistungsfähigkeit individueller gestaltet werden kann.
Der Kliniker teilt die schweren Formen einer COPD häufig in zwei Phänotypen ein, obwohl nicht selten Mischbilder dieser Typen vorliegen
Pink Puffer
Beim Pink Puffer („rosa Schnaufer“) handelt es sich um einen Typ mit hagerem Erscheinungsbild ("pulmonale Kachexie"), starker Luftnot und eher trockenem Husten. Diese Patienten haben nur selten eine leichte Zyanose [Blauverfärbung des Blutes (z. B. auch der Lippen), das weniger Sauerstoff trägt], da durch kompensatorische Atemarbeit weniger Sauerstoffmangel bestehen.
Blue Bloater
Beim Blue Bloater („blauer Aufgedunsener“) handelt es sich charakteristischerweise um Patienten mit Übergewicht, die unter Husten und wechselnd viel Auswurf leiden. Trotz einer ausgeprägten Zyanose mit erheblichem Sauerstoffmangel ist die Atemnot weniger ausgeprägt. Seinen Sauerstoffmangel toleriert der „Blue Bloater“ besser als der „Pink Puffer“ und reagiert auch mittels vermehrter Bildung roter Blutkörperchen (Polyglobulie). So kann bei niedrigerem Sauerstoffangebot trotzdem mehr Sauerstoff transportiert werden, weil mehr Hämoglobin vorhanden ist.
Klinisch bedeutsam ist die Differenzierung zwischen COPD und Asthma. Neun Merkmale erleichtern die Differenzialdiagnostik der beiden häufigsten obstruktiven Atemwegserkrankungen und sind in der folgenden Tabelle 3 zusammengefasst:

Tabelle 3 aus S3-Leitlinie COPD (Atemwegsliga oder Pneumologie 2007; 61; e1_e40)
In der nationalen Versorgungsleitlinie Asthma wird diese Erkrankung definiert als eine chronisch entzündliche Erkrankung der Atemwege, charakterisiert durch eine bronchiale Hyperreagibilität und eine variable Atemwegsobstruktion. Asthma ist eine der häufigsten chronischen Erkrankungen, die bei ca.10 % der kindlichen und 5 % der erwachsenen Bevölkerung in Deutschland vorkommt. Mehrere Formen von Asthma werden unterschieden: Allergien sind der stärkste prädisponierende Faktor bei der Entwicklung eines Asthmas im Kindes- und Jugendalter, doch auch beim Erwachsenen sind Allergien in 50-80 % der Fälle primär ursächlich. Das allergische Asthma wird vom intrinsischen oder nicht allergischen Asthma und Sonderformen wie dem Aspirin-sensitiven Asthma abgegrenzt. Beim intrinsischen Asthma spielen Infektionen der Atemwege eine ursächliche Rolle. Mischformen sind möglich. So kann bei einem initial allergischem Asthma im Verlauf die intrinsische Komponente klinisch in den Vordergrund treten.
Die drei wichtigsten Charakteristika in der Differenzialdiagnostik von Asthma und COPD sind das klinische Bild, die oft komplette Reversibilität der Bronchialobstruktion und die variable bronchiale Hyperreaktivität. Erste Anhaltspunkte liefert die Anamnese: Asthma macht sich meist im Kindes- und Jugendalter bemerkbar, die COPD beginnt typischerweise erst in der zweiten Lebenshälfte und entwickelt sich schleichend.
Asthma fällt klinisch durch anfallsartig auftretende Atemnot und/oder Hustenattacken auf. Chronischer Husten kann die alleinige Manifestation darstellen. Dann spricht man vom Husten als Asthmaäquivalent. Die Lungenfunktionsanalyse ergibt bei Asthma eine partielle oder vollständig reversible Bronchialobstruktion nach Gabe von Bronchodilatatoren sowie eine relevante bronchiale Hyperreagibilität. Die vollständige Reversibilität der Obstruktion schließt eine leichte COPD zwar nicht aus, spricht aber im Regelfall für Asthma. Asthmatiker erleben einen häufigen und oft saisonalen Wechsel zwischen gesünderen und kränkeren Phasen, die COPD hat einen progredienten Verlauf mit kontinuierlicher oder in Schüben verlaufender Verschlechterung. Die Schübe werden auch Exazerbationen genannt. Patienten mit Merkmalen beider Erkrankungen können der Kombination aus Asthma und COPD zugeordnet werden. Die Behandlung sollte dem jeweiligen Schweregrad beider Erkrankungen und bei dem COPD dem Exazerbationsmuster und den Begleiterkrankungen angepasst werden.
Prof. Dr. Helmut Teschler, Facharzt für Innere Medizin, Lungen- und Bronchialheilkunde, Allergologie, Schlafmedizin sowie Chefarzt der Pneumologie Ruhrlandklinik - Westdeutsches Lungenzentrum am Universitätsklinikum Essen, (6. Symposium Lunge in Hattingen/NRW)
Abdruck bzw. die Weiterverwertung dieses Artikels oder Teilen daraus in Print- oder Onlinemedien bedürfen der vorherigen schriftlichen Genehmigung des COPD-Deutschland e.V.
